 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
配制pH为2.00和10.00的氨基乙酸缓冲溶液各100mL,其缓冲物质总浓度为0.10mol·L-1,问需分别称取氨基乙酸(NH2C
配制pH为2.00和10.00的氨基乙酸缓冲溶液各100mL,其缓冲物质总浓度为0.10mol·L-1,问需分别称取氨基乙酸(NH2CH2COOH)多少克?加0.1mol·L-1HCl和1.0mol·L-1NaOH各多少mL?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
配制pH为2.00和10.00的氨基乙酸缓冲溶液各100mL,其缓冲物质总浓度为0.10mol·L-1,问需分别称取氨基乙酸(NH2CH2COOH)多少克?加0.1mol·L-1HCl和1.0mol·L-1NaOH各多少mL?
 答案
答案
 更多“配制pH为2.00和10.00的氨基乙酸缓冲溶液各100mL,其缓冲物质总浓度为0.10mol·L-1,问需分别称取氨基乙酸(NH2C”相关的问题
更多“配制pH为2.00和10.00的氨基乙酸缓冲溶液各100mL,其缓冲物质总浓度为0.10mol·L-1,问需分别称取氨基乙酸(NH2C”相关的问题
第1题
配制氨基乙酸总浓度为0.10mol·L-1的缓冲溶液(pH=2.0)100mL,需氨基乙酸多少克?还需加多少毫升1.0mol·L-1酸或碱,所得溶液的缓冲容量为多大?
第2题
计算下列溶液的pH
(1)50℃纯水和100℃纯水;
(2)0.20mol·L-1HClO4;
(3)4.0x10-3mol·L-1Ba(OH)2;
(4)将S0mL0.10mol·L-1HI稀释至1.0L;
(5)将100mL2.0x10-3mol·L-1HCl和400mLI.0x10-3mol·L-1HCIO2混合;
(6)混合等体积的0.20mol·L-1HCI和0.10mol·L-1NaOH;
(7)将pH为8.00和10.00的NaOH溶液等体积混合;
(8)将pH为2.00的强酸和pH为13.00的强酸碱溶液等体职混合.
第4题
(1)实际上所配缓冲溶液的pH为多少?
(2)若要配制pH=0.64三氯乙酸缓冲溶液。需加入多少摩尔强酸或强碱?
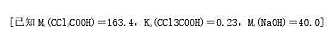
第5题
用0.1000mol·L-1NaOH溶液滴定50.00mL一元弱酸的数据如下:
(a)绘制滴定曲线;
(b)绘制 曲线;
曲线;
(c)用二级微商法确定终点;
(d)计算试样中弱酸的浓度;
(e)化学计量点的PH应为多少?
(f)计算此弱酸的电离常数(提示:根据滴定曲线上的半中和点的PH)。
| 体积/mL | pH |
| 0.00 1.00 2.00 4.00 7.00 10.00 12.00 14.00 15.00 15.50 15.60 15.70 15.80 16.00 17.00 20.00 24.00 28.00 | 3.40 4.00 4.50 5.05 5.47 5.85 6.11 6.60 7.04 7.70 8.24 9.43 10.03 10.61 11.30 11.96 12.39 12.57 |
第6题
A.2.00
B.3.00
C.10.00
D.20.00
E.30.00
第7题
A.0.010%~0.500%
B.0.050%~2.00%
C.0.015%~5.00%
D.0.050%~10.00%
第8题
同样地,如果美国1单位C的市场价格为2美元,那么,相应的工人的小时工资应为(0.30美元/0.60美元/2.00美元/10.00美元/12.00美元)。
第10题
A.羟氨(NH2OH)Kb=1×10-9
B.氨水Kb=1×10-5
C.甲酸Ka=1×10-4
D.乙酸Ka=1×10-5