 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
粗盐提纯时,如何除去粗盐溶液中的Mg2+,Ca2+和SO42-?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“粗盐提纯时,如何除去粗盐溶液中的Mg2+,Ca2+和SO42-?”相关的问题
更多“粗盐提纯时,如何除去粗盐溶液中的Mg2+,Ca2+和SO42-?”相关的问题
第2题
A.二氧化碳的实验室制取与性质
B.粗盐的提纯
C.配制一定浓度的溶液,比较不同浓度溶液的某些性质差异
D.收集不同的水样,测定其pH,并用图表或数据等表示实验结果
第5题
下面是某教师“粗盐提取”的教学片段实录。
学生实验1:用托盘天平称取5.09粗盐,用药匙将该粗盐逐渐加入盛有10 mL水的烧杯里,边加边用玻璃棒搅拌,直加到粗盐不再溶解为止。
教师提问1:玻璃棒起什么作用?观察所得食盐水是否浑浊。
学生讨论1:得出结论。
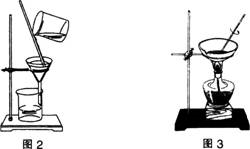
学生实验2:过滤食盐水(图2),仔细观察滤纸上的剩余物及滤液的颜色,如滤液仍浑浊,再过滤一次。
教师提问2:如果两次过滤后滤液仍浑浊,应如何检查实验装置并找出原因?
学生讨论2:得出结论。
学生实验3:把所得澄清滤液倒入蒸发皿。把蒸发皿放在铁架台的铁圈上,用酒精灯加热,同时用玻璃棒不断搅拌滤液。(图3)
教师提问3:加热过程为什么用玻璃不断搅拌滤液?
学生讨论3:得出结论。
问题:
(1)上述教学过程中体现了哪些课程理念?(可从知识建构、能力发展、科学方法、科学精神、动机培养等5个方面。任选3个方面予以回答)
(2)在该教学片段中老师是如何达成“过程与方法”教学目标的?
(3)图2实验需注意的事项有哪些?如果两次过滤后滤液仍浑浊,分析可能的原因有哪些?图3中为什么要用玻璃棒不断搅拌滤液?
(4)在该内容的后续教学中,学生讨论得出“粗盐中含有的杂质只有泥沙等不溶的物质,通过过滤、蒸发即可得到纯净的NaCl”。判断该结论是否正确,并分析为什么?
第6题
如何鉴别和提纯下列化合物?
(1)区别萘、喹啉和8-羟基喹啉;
(2)区别吡啶和喹啉;
(3)除去混在苯中的少量噻吩;
(4)除去混在甲苯中的少量吡啶;
(5)除去混在吡啶中的少量六氢吡啶。
第7题
下列属于利用“结晶”原理进行操作的方法是()。
A.把粗盐倒入水中,经过搅拌后水变浑浊了
B.静置一段时间,粗盐水变得干净透明了
C.把盐水倒入装有滤纸的杯子里
D.把盐水放在阳光下使水蒸发
第8题
溶液中Mg2+的浓度为2.0×10-2mol/L,问:(1)pH=5.0时,能否用EDTA准确滴定Mg2+?(2)在pH =10.0时,情况如何?(3)继续升高pH情况又如何?
第9题
(1)为什么不用直接沉淀出Fe(OH)2的方法提纯CuCl2?
(2)该厂所采用去除铁杂质方法的可行性.
第10题
A.瘦肉风干发酵时其酸碱值降低,导致其中肌红蛋白被氧化,血红素分解,染红整根香
B.肥肉富含饱和脂肪酸,经发酵氧化后释放出复合红色素,油脂液化,使红色素均匀分布
C.肠衣在保护肠肉的同时,自身水分逐渐丢失,表面上的红霉菌较为均匀地繁殖,经紫外线照射分解死亡,留下润泽的“红斑”
D.肠内的粗盐、料酒等调料本身具有淡黄、淡红等颜色,经乳酸菌发酵,红色素会不断沉淀
第11题
用镁离子选择电极测定溶液中的Mg2+,其电池的组成为
镁离子选择电极|Mg2+||饱和甘汞电极
在25℃时,c(Mg2+)=1.15×10-2mol·L-1时,该电池的电动势为0.275V,当用Mg2+试液代替已知溶液时,测得电动势为0.280V,计算试液的pMg。