 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有一种白色固体,将其溶于水后进行下列实验,请根据实验现象写出此白色固体的化学式,并给出相关
①用铂丝蘸少量液体在火焰上灼烧,产生黄色火焰。
②它使酸化的KMnO4溶液褪色而产生无色溶液,此溶液与BaCl2溶液作用生成不溶于稀HNO3的白色沉淀。
③加入硫粉,并加热,硫溶解生成无色溶液,此溶液酸化时产生乳白色或浅黄色沉淀,此溶液也能使KI3溶液褪色,并能溶解AgBr。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
①用铂丝蘸少量液体在火焰上灼烧,产生黄色火焰。
②它使酸化的KMnO4溶液褪色而产生无色溶液,此溶液与BaCl2溶液作用生成不溶于稀HNO3的白色沉淀。
③加入硫粉,并加热,硫溶解生成无色溶液,此溶液酸化时产生乳白色或浅黄色沉淀,此溶液也能使KI3溶液褪色,并能溶解AgBr。
 答案
答案
 更多“有一种白色固体,将其溶于水后进行下列实验,请根据实验现象写出此白色固体的化学式,并给出相关”相关的问题
更多“有一种白色固体,将其溶于水后进行下列实验,请根据实验现象写出此白色固体的化学式,并给出相关”相关的问题
第1题
第2题
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
第3题
案例:
梁老师安排同学们分组进行生石灰与水反应的实验,大家都观察到如下现象:
①将水滴到生石灰上,过十几秒后才开始反应;
②生石灰块状固体碎裂:
③有白色“烟雾”生成并向空中上升:
④有“哧哧”的声音,水沸腾了。
经过讨论.大家对反应的原理、放热的现象都取得了一致的意见,但对实验中上升的白色“烟雾,,存在疑问.“这白色烟雾是什么呢?…‘为什么又会在空气中上升呢?”同学们议论纷纷。梁老师认为,这是一个培养学生探究能力的好机会,有必要调整一下教学计划,让同学们自己展开对这一问题的探究。于是提出了问题:
“同学们.根据这些现象你认为白色‘烟雾’的成分可能是什么?”
同学们纷纷提出自己的见解.大致有3种意见:
①白色“烟雾”可能是水蒸气凝结成的小水滴;
②白色“烟雾”可能是随热气飘出的氢氧化钙固体小颗粒;
③白色“烟雾”也可能既含有小水滴又含有氢氧化钙固体小颗粒。
粱老师进一步引导探究:“请根据你的假设,设计并动手进行实验,证明你的猜测。”
顿时,教室里一片议论声,同学们积极动手开始了实验。大约过了十几分钟,看到多数同学已完成了实验,梁老师建议大家停下来,请各组谈谈自己设计的实验、观察到的现象及得出的结论。
“我们将一只干燥的小烧杯罩在白色烟雾上,烧杯上出现了水滴,所以,我们认为是水蒸气。” “你们没有认真观察”,另一组同学马上插话,“我们用的是玻璃片,除了水滴,还有白色粉末,连我拿玻璃片的手上都有了。”
“我们还向小烧杯中加了点水,又滴入了酚酞,结果变成红色的了。”
问题:
(1)你认为上述实验中白色“烟雾”的成分可能是什么?为什么会在空气中上升?
(2)2述案例中,梁老师运用了哪些教学方法?
(3)上述案例中,梁老师的做法体现了哪些教学理念?
第4题
推理判断:
(1)无色晶体(A)在电炉高温下与碳反应得到灰黑色单质(B),(B)与浓氢氧化钠溶液共热生成无色气体(C)和物质(D)的溶液。气体(C)可以使灼热的黑色氧化铜变成单质铜。(A)与氢氟酸作用有气体(E)生成,(E)通水中生成白色沉淀(F)和气体(G),(G)与过量反应物(E)化合得(H)的溶液。(H)的溶液与过量氯化钾作用可以结晶出(1)。(A)与碳酸钠共熔生成物质(D),(A)与炭粉共热的体系通氧气有无色液体(J)生成,(J)与水反应可得(F)。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)的化学式,并完成各步的化学反应方程式。
(2)蓝黑色化合物(A)不溶于水,但可溶于稀盐酸生成(B)的溶液,稀释该溶液时,析出白色沉淀(C),酸化时.沉淀溶解。向(B)的溶液中通硫化氢时,生成灰黑色沉淀(D),该沉淀可溶于浓盐酸。(D)与硝酸反应时产生浅黄色沉淀(E),无色气体(F)和化合物(C)的溶液。(F)在空气中迅速变成红棕色。向(G)的溶液中通硫化氢时,生成黄色沉淀(H)。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
(3)金属单质(A)与氯气在加热时反应生成无色液体(B),(B)经金属(A)处理转变为固体化合物(C)。向(C)的盐酸溶液中通入硫化氢气体生成灰黑色沉淀(D),(D)不溶于硫化钠溶液,但可溶于过硫化钠溶液形成(E)的溶液。向(E)的溶液中加入盐酸生成黄色沉淀(F),并有气体(G)放出。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(4)红色化合物(A)经稀硝酸处理后得到黑色沉淀物(B)和无色透明溶液,从该溶液中可以结晶出无色品体(C)。晶体(C)加热时放出红棕色气体(D)。(B)在酸性介质中与二价锰离子作用,溶液逐渐变为紫红色,说明有化合物(E)生成。若向(C)的水溶液中滴稀盐酸有白色沉淀(F)生成,(F)不溶于氨水;若向(C)的水溶液中滴碘化钾溶液,则生成黄色沉淀(G);若向(C)的水溶液中滴加氢氧化钠溶液,有白色沉淀(H)生成,氢氧化钠过量则沉淀消失。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
(5)物质(A)为黄灰色固体,与水反应得白色沉淀(B)、气体(C)及无色溶液。(B)可以溶于氢氧化钠溶液,若与氧化物(D)作用将生成(E)和水。(B)受热脱水生成(F),经过高温灼烧的(F)既不溶于酸,也不溶于碱,但与焦硫酸钾共熔可得两种能溶于水的化合物,其中一种是(E)。将气体(C)通入硝酸铅溶液得黑色沉淀(G),(G)与臭氧反应转化为白色固体(H)。
试给出(A),(B),(C),(D),(E),(F),(G)和(H)的化学式,并完成各步的化学反应方程式。
第5题
阅读下列三段材料,根据要求完成任务。
材料一《普通高中化学课程标准(实验)》关于金属及其化合物的内容标准:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要应用。
材料二某版本高中实验教科书《化学l》“铝的重要化合物”的内容:二、铝的重要化合物
铝是地壳中含量最多的金属元素,但人们发现并制得单质铝却比较晚,这是由于铝很活泼.从铝的化合物中提炼铝单质比较困难。铝的许多化合物在人类的生产和生活中具有重要的作用。
1.氧化铝
我们已经知道,氧化铝难溶于水,熔点很高,也很坚固,因此覆盖在铝制品表面极薄的一层氧化铝就能有效地保护内层金属。氧化铝是冶炼金属铝的原料,也是一种比较好的耐火材料。
它可以用来制造耐火坩埚、耐火管和耐高温的实验仪器等。
氧化铝难溶于水,却能溶于酸或强碱溶液中。它溶于碱时,生成物是偏铝酸盐和水。因此,氧化铝是一种两性氧化物。
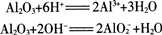
2.氢氧化铝【实验3-7】
在试管里加入l0 mL 0.5 mol/L Al2(S04)3溶液,滴加氨水,生成白色胶状物质。继续酒加氨水.直到不再产生沉淀为止。
反应中得到的白色胶状物质是氢氧化铝[AI(OH)3],它几乎不溶于水,但能凝聚水中的悬浮物.并能吸附色素。在实验室里,常常用铝盐溶液与氨水反应来制取氢氧化铝。
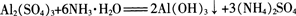
【实验3-8】
取一些上面实验中制得的AI(OH),沉淀,分装在2支试管里,往一支试管里滴加2 mol/L盐酸.往另一支试管里滴加2 mol/L NaOH溶液。边加边振荡,观察现象。
实验证明,AI(OH)3在酸或强碱溶液里都能溶解。这说明它既能与酸起反应,又能与强碱起反应.它是两性氢氧化物。
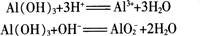
AI(OH)3是医用的胃酸中和剂中的一种,它的碱性不强,不至于对胃壁产生强烈的刺激或腐蚀作用,但却可以与酸反应,使胃液酸度降低,起到中和过多胃酸的作用。
加热时,AI(OH)3分解为氧化铝和水。
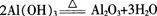
【学与问】
问题:为什么常用氨水与硫酸铝溶液反应制取氢氧化铝,而不用氢氧化钠溶液?
材料三教学对象为高中一年级学生,他们已经学习了必修化学1的“铝单质”“物质的分类”以及“离子反应”等知识。
要求:
(1)回答材料二“学与问”中的问题。
(2)完成“铝的重要化合物’’的教学设计片段,内容包括教学目标、教学方法和教学过程。
第6题
推理判断:
某盐(A)与盐酸反应,生成(B)的溶液和气体(C)。向(B)的浓溶液中加锑酸钾,析出白色晶状沉淀(D)。将气体(C)通入碘化钾溶液,生成(E)和(F),(E)使溶液发黄,(F)与过量硝酸铅生成白色沉淀(C),(G)溶于过量氢氧化钠溶液得(H),(H)与(A)反应生成黑色沉淀(I)。(I)加到硫酸锰溶液中可使溶液变成紫红色,说明有离子(J)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)的化学式,并完成各步的化学反应方程式。
(2)白色固体(A)高温下分解成(B)和气体(C)。白色固体(B)与碳在更高的温度下共热生成(D),灰黑色固体(D)与水作用生成重要工业燃气(E)和化合物(F)。(B)与稀盐酸反应生成(G)的溶液。电解(G)的无水熔盐得(H)和气体(I)。金属(H)在高温下与(J)化合成为(K),白色晶体(K)与水反应的产物中有(F)。气体(J)在(I)中燃烧的产物溶于水得盐酸。(D)在高温下与水蒸气作用,其固体产物为(A),气体产物为(C)和(J)。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I),(J)和(K)的化学式,并完成各步的化学反应方程式。
第7题
A.少量有机、无机有毒气体的实验应打开通风设备,排出窗外
B.实验所产生的对环境有污染的废液应分类倒入指定容器储存
C.酸性、碱性废液按其化学性质,分别进行中和后处理,使pH值达到在6-9之间后排放
D.不溶于水的废弃化学药品禁止丢进废水管道中,集中收集后放入纸篓内,及时倾倒
第8题
)中滴加适量NaOH溶液得白色沉淀(D),加入过量NaOH溶液时,(D)溶解得无色溶液(E)。向(E)中加入NaClO溶液并微热,有棕黑色沉淀(F)生成。将(F)洗净后在一定温度下加热又得(A)。用硝酸处理(A)得沉淀(F)和溶液(C)。向(F)中加入盐酸有白色沉淀(G)和气体(H)生成,(H)可使淀粉碘化钾试纸变蓝。将(G)和KI溶液共热,冷却后有黄色沉淀(Ⅰ)生成。试给出(A),(B),(C),(D),(E),(F),(C),(H)和(I)所代表的物质的化学式,并写出有关化学反应方程式。
第9题
A.国际社会将稀土视为一种战略资源
B.它是钢铁、有色金属、石油等产业的重要原料
C.它在光电信息等高技术领域中有不可替代的作用
D.中国是第一大稀土资源国。是能够提供全部17种稀土金属的国家之一
第10题
入硝酸和少量NaBiO3(s),生成紫红色溶液(D).在(D)中加入一淡绿色溶液(E),紫红色褪去,在得到的溶液(F)中加入KNCS溶液又生成血红色溶液(C).再加入足量的NaF则溶液的顏色又褪去.在(E)中加入BaCl2溶液则生成不溶于硝酸的白色沉淀(H).试确定各字母所代表的物质,并写出有关的离子方程式.
第11题
A.国际社会将稀土视为一种战略资源
B.它是钢铁、有色金属、石油等产业的重要原料
C.它在光电信息等高技术领域中有不可替代的作用
D.中国是第一大稀土资源国.是能够提供全部l7种稀土金属的国家之一