 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
下列电池的电动势为0.413V,,计算弱酸HA的解离常数。
下列电池的电动势为0.413V,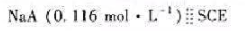 ,
,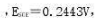 计算弱酸HA的解离常数。
计算弱酸HA的解离常数。
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列电池的电动势为0.413V,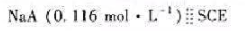 ,
,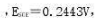 计算弱酸HA的解离常数。
计算弱酸HA的解离常数。
 答案
答案
 更多“下列电池的电动势为0.413V,,计算弱酸HA的解离常数。”相关的问题
更多“下列电池的电动势为0.413V,,计算弱酸HA的解离常数。”相关的问题
第3题
为了测定CuY2-的稳定常数,组成下列电池:
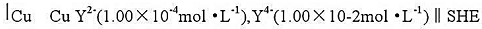
25℃时,测得电池电动势为0.227V,计算KcuY2-
第4题
测得下列电池的电动势为0.873V(25℃)
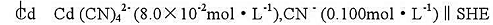
试计算Cd(CN)42-的稳定常数.
第6题
25℃时,下列电池的电动势为0.518V(忽略液接电位):
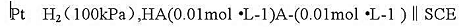
计算弱酸HA的Ka值.
第7题
下列电池的电动势为0.048V,计算AgI的溶度积常数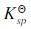 =?
=?
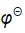 (Ag[+/Ag)=+0.799V]
(Ag[+/Ag)=+0.799V]
(-)Ag,AgI(s)|NaI(0.020mol·L-1)||H+(a=1mol·L-1)|H2(101.325kPa)|Pt()。
第8题
在下列电池中Pt,H2(101.3kPa),HAc(xmol.L-1),Ac一(ymol.L-1)SCE当电池的电动势为0.620 V时,计算溶液中[HAe]和[NaAc]的比值为多少(25℃)?(已知E(SCE)=0.242 V,醋酸的pKa=4.74)
第9题
当下列电池中的溶液是pH=4.00的缓冲溶液时,在25℃测得电池的电动势为0.209V:玻璃电极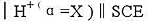 当缓冲溶液由未知溶液代替时,测得电池电动势如下:
当缓冲溶液由未知溶液代替时,测得电池电动势如下:
(a)0.312V; (b)0.088V; (c)-0.017V.试计算每种溶液的pH.
第10题
(1)写出电池反应方程式;
(2)由附表六查得Eθ(Cl2/Cl-),计算E(Co2+/Co);
(3)p(Cl2)增大时,电池的电动势将如何变化?
(4)当CO2+浓度为0.010mol·L-1其他条件不变时,电池的电动势是多少伏?