 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在含有KI和KBr的混合溶液中通入过量的Cl2,将溶液蒸干并灼烧,最后剩余的是()
A.I2和KCl
B.KCl
C.r2和KCl
D.KCl和KBr
 答案
答案
B、KCl
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.I2和KCl
B.KCl
C.r2和KCl
D.KCl和KBr
 答案
答案
B、KCl
 更多“在含有KI和KBr的混合溶液中通入过量的Cl2,将溶液蒸干并灼烧,最后剩余的是()”相关的问题
更多“在含有KI和KBr的混合溶液中通入过量的Cl2,将溶液蒸干并灼烧,最后剩余的是()”相关的问题
第1题
称取含有苯酚的试样0.5000g,溶解后加入0.1000mol/L KBrO3溶液(其中含有过量KBr)25.00mL,并加HCl酸化,放置。待反应完全后,加入KI。滴定析出的I2消耗了0.1003mol/L的Na2S2O3溶液29.91mL。计算试样中苯酚的含量。
第2题
取一含KI和KBr的样品1.000g,溶解于水中并稀释至200.0mL,取其50.00mL,在中性介质中用Br2处理,以使I-变成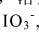 ,过量的Br2用沸腾法除去。再加入过量的KI溶液,酸化后,生成的I2用0.05000mol/L Na2S2O3溶液滴定,消耗40.80mL。另取50.00mL被测溶液,用K2Cr2O7强酸性溶液氧化,释放出来的I2和Br2被蒸馏出来,并收集在较浓的KI溶液中,再用Na2S2O3溶液滴定,消耗29.80mL,计算原样品中KI和KBr的含量。
,过量的Br2用沸腾法除去。再加入过量的KI溶液,酸化后,生成的I2用0.05000mol/L Na2S2O3溶液滴定,消耗40.80mL。另取50.00mL被测溶液,用K2Cr2O7强酸性溶液氧化,释放出来的I2和Br2被蒸馏出来,并收集在较浓的KI溶液中,再用Na2S2O3溶液滴定,消耗29.80mL,计算原样品中KI和KBr的含量。
第3题
间后加入BaCl2溶液有白色沉淀(C)生成,(C)不溶于强酸。(A)的溶液与MnSO4混合后加稀硝酸和几滴AgNO3溶液,加热,溶液变红,说明有(D)生成。(A)的溶液与KOH混合后加热,有气体(E)放出。气体(E)通入AgNO3溶液则有棕黑色沉淀(F)生成,(E)通入过量则沉淀溶解为无色溶液。试给出(A),(B),(C),(D),(E)和(F)所代表的物质的化学式,并用化学反应方程式表示各过程。
第4题
A.两电对BrO3-/Br-与I2/2I-的电位相等
B.反应产物I2与KBr的物质的量相等
C.溶液中已无BrO3-离子存在
D.反应中消耗的KBrO3的物质的量与产物I2的物质的量之比为1:3
E.反应中消耗的KBrO3的物质的量与产物I2的物质的量之比为1:2
第5题
取一定量的MnO2固体,加入过量浓HCl,将反应生成的Cl2通入KI溶液,游离出I2,用0.1000mol·L-1Na2S2O3滴定,耗去20.00mL,求MnO2的质量。
第6题
第7题
放出,同时溶液中有白色沉淀(C)析出。(C)在空气中迅速变为灰绿色,黑色,最后变为红棕色沉淀(D)。(D)溶于稀盐酸中生成棕黄色溶液(E)。向溶液(E)中滴加KI溶液,先有褐色沉淀(F)析出,随后变为红棕色溶液(G)。若在滴加KI溶液之前先加入过量KF溶液,则无此现象。向(D)的浓NaOH悬浮液中通入氯气,可得到紫红色溶液(H)。在(A)溶液和(H)溶液中分别滴加BaCl2溶液,均可析出沉淀,但前者是白色沉淀(I),后者是紫红色沉淀(J)。沉淀(I)不溶于HNO3,但(J)遇HNO3即分解并放出(K)。试给出(A),(B),(C),(D),(E),(F),(G),(H),(I),(J)和(K)所代表的物质的化学式,并用化学反应方程式表示各过程。
第8题
试写出下列反应的化学方程式,并叙述实验现象:
(1)单质碘溶于在碘化钾溶液中;
(2)在碘化钾溶液中不断通入氯气,直至过量;
(3)少量硫粉与氯酸钾混合均匀后慢慢研磨;
(4)在硝酸汞溶液中逐滴加人碘化钾,直至过量;
(5)高碘酸在酸性条件下与二价锰离子反应;
(6)向次氯酸钠溶液中加入几滴硫酸锰。
第9题
称取含NaIO3和NaIO4的混合试样1.000g,溶解后定容于250mL容量瓶中;准确移取试液50.00mL,调至弱碱性,加入过量KI,此时IO4-被还原为IO3-(IO3-不氧化I-);释放出的I2用0.04000mol/L Na2S2O3溶液滴定至终点时,消耗10.00mL。另移取试液20.00mL,用HCl调节溶液至酸性,加入过量的KI;释放出的I2用0.04000mol/LNa2S2O3溶液滴定,消耗30.00mL。计算混合试样中NaIO3和NaIO4的含量。
第10题
A.饱和石灰水中通过量CO2
B.AlCl3溶液中通过量NH3
C.MgCl2、AlCl3混合溶液中逐滴滴加NaOH溶液至过量
D.含少量HCl的AlCl3溶液中逐滴滴加NaOH溶液至过量
第11题
A.反离子是
C.扩散层带负电 D.溶胶是负溶胶