 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有500毫升未知浓度的盐酸溶液,取10毫升用0.1mol£¯L(NaOH)氢氧化钠溶液滴定,滴定时滴过了理论终点,共加了12.5毫升NaOH溶液。因此,将此溶液用0.01mol£¯L(HCl)盐酸中和时耗去了0.01mol£¯L(HCl)盐酸5毫升,问盐酸原始浓度?并且在500毫升原始盐酸中所含的氯化氢是多少?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“有500毫升未知浓度的盐酸溶液,取10毫升用0.1mol£¯L(NaOH)氢氧化钠溶液滴定,滴定时滴过了理论终点,共加了12.5毫升NaOH溶液。因此,将此溶液用0.01mol£¯L(HCl)盐酸中和…”相关的问题
更多“有500毫升未知浓度的盐酸溶液,取10毫升用0.1mol£¯L(NaOH)氢氧化钠溶液滴定,滴定时滴过了理论终点,共加了12.5毫升NaOH溶液。因此,将此溶液用0.01mol£¯L(HCl)盐酸中和…”相关的问题
第1题
称取硼砂(Na2B4O7·10H2O)0.4853g,用以标定盐酸溶液。已知化学计量点时消耗盐酸溶液24.75mL,求此盐酸溶液的物质的量浓度。
第2题
配制c(NaOH)=0.10mol·L-1的溶液300mL,计算需用固体NaOH的质量。取这种溶液20.00mL,恰好与25.00mL的盐酸完全中和,计算此盐酸的浓度。
第3题
0.0mL比色管内用邻二氮菲显色,定容后在510nm处测得吸光度如下:

取1.00mL含Fe2+未知溶液稀释到100.00mL,再取稀释液5.00mL,在50.0mL比色管内用同样方法显色定容后测得吸光度A=0.47.求未知溶液中Fe2+的浓度.
第4题
用去盐酸体积20.54mL,计算盐酸的浓度为多少mol/L?已知M(Na2CO3)=105.99g/mol。
第5题
响)?
(1)滴定速度太快,附在滴定管壁上的盐酸来不及流下来就读取滴定体积;
(2)称取Na2CO3时,实际质量为0.1238g,记录时误记为0.1248g;
(3)在将盐酸标准溶液倒入滴定管之前,没有用盐酸淋洗滴定管;
(4)使用的Na2CO3中含有少量的NaHCO3。
第6题
下表加入不同量的10μg·mL-1Fe2+标准溶液,再加1.0mL 100g·L-1盐酸羟胺溶液(用以将试液中Fe3+还原为Fe2+),2.0mL 1.5g·L-1邻二氮菲(与铁形成橘红色配合物)和5.0mL 1mol·L-1NaAc溶液(为减少其他离子干扰,以控制pH≈5的溶液中显色)再用水稀释至刻度,在510nm处测定吸光度,试计算试液中Fe的浓度?
| 编 号 | 空白 | 1 | 2 | 3 | 4 | 5 |
| 未知试液/mL | 0.0 | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 |
| 10μg·mL-1Fe2+标准溶液/mL | 0.0 | 0.0 | 10.0 | 15.0 | 20.0 | 25.0 |
| 吸光度A | 0.040 | 0.201 | 0.291 | 0.341 | 0.381 | 0.432 |
第7题
用荧光分析比较法测定食品中维生素B1的含量,其标准溶液浓度为8.0mg·L-1时,测得荧光强度为24.0。取样品2.00g,溶于100.0mL盐酸中,测定荧光强度为20.0,空白溶液的荧光强度为4.0。计算样品中维生素B1的含量。
第8题
电池: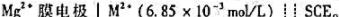 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。
(1)当用未知溶液代替上述已知Mg2+溶液时。测得电池电动势为0.425V,求此溶液的pMg为多大?
(2)若溶液替代引起液接电位Ej的不稳定值为±1mV,则Mg2+浓度测定产生的相对误差有多大?波动范围为多少?
第9题
若同类旋光性溶液的厚度分别为L1、L2已知,浓度C1、C2分别为已知和未知,其旋光角φ1、φ2可测出,则未知溶液浓度C2为______。
第10题
有一碱液,可能是NaOH、NaHCO3或Na2CO3或它们的混合物溶液。今用盐酸标准溶液滴定,若以酚酞为指示剂,耗去盐酸的体积为V1;若取同样的该碱液,也用盐酸标准溶液滴定,但以甲基橙为指示剂,耗去盐酸的体积为V2。试由V1与V2的关系判断碱液的组成:
第11题