 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某盐酸标准溶液每毫升溶液含4.374×10-3gHCl,试计算:①该盐酸标准溶液对NaOH的滴定度;②对CaO的滴定度。(已知MHCl=36.46,MNaOH=40.00,MCaO=56.08。)
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“已知某盐酸标准溶液每毫升溶液含4.374×10-3gHCl,试计算:①该盐酸标准溶液对NaOH的滴定度;②对CaO的滴定度。(已知MHCl=36.46,MNaOH=40.00,MCaO=56.08。)”相关的问题
更多“已知某盐酸标准溶液每毫升溶液含4.374×10-3gHCl,试计算:①该盐酸标准溶液对NaOH的滴定度;②对CaO的滴定度。(已知MHCl=36.46,MNaOH=40.00,MCaO=56.08。)”相关的问题
第1题
漂白粉中“有效氨”可用亚砷酸钠法测定;
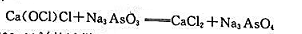
现有含“有效氧”29.00%的试样0.3000g,用25.00cm3Na3AsO3溶液恰能与之作用。每毫升Na3AsO3,溶液含多少克的砷?同样质量的试样用碘量法测定,需用Na2S2O3标准溶液[T(CuSO4·5H2O/Na2S2O3)=0.01250g·cm-3]多少毫升?
第2题
,以磺基水杨酸为指示剂。用0.02000mol·L-1EDTA标准溶液滴定试样中的Fe3+。用去18.16ml.然后将试液调至pH=3.5,加入上述EDTA标准溶液25.0mL,并加热煮沸。再调试液pH=4.5.以PAN为指示剂,趁热用CuSO4标准溶液(每毫升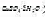 为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
第3题
称取某有机试样0.1084g测定其中的含磷量。将试样处理成溶液,并将其中的磷氧化成 ,加入其他试剂使之形成MgNH4PO4沉淀。沉淀经过滤洗涤后,再溶解于盐酸中并用NH3-NH4Cl缓冲溶液调至pH=10,以EBT为指示剂,需用0.01004mol/L的EDTA标准溶液21.04mL滴定至终点,计算试样中磷的质量分数。
,加入其他试剂使之形成MgNH4PO4沉淀。沉淀经过滤洗涤后,再溶解于盐酸中并用NH3-NH4Cl缓冲溶液调至pH=10,以EBT为指示剂,需用0.01004mol/L的EDTA标准溶液21.04mL滴定至终点,计算试样中磷的质量分数。
第4题
称取0.5000g黏土样品,用碱熔后分离去SiO2,用容量瓶配成250mL溶液。吸取100mL试液,在pH=2~2.5的热溶液中,用磺基水杨酸作指示剂,用0.02000mol/L的EDTA标准溶液滴定Fe3+,用去7.20mL。滴定Fe3+后的溶液,在pH=3.0时,加入过量的EDTA溶液,再调至pH=4~5.0煮沸,用PAN作指示剂,以CuSO4标准溶液(每毫升含CuSO4·5H2O为0.00500g)滴定至溶液呈紫红色。再加入NH4F煮沸后,又用CuSO4标准溶液滴定,用去CuSO4标准溶液25.20mL。试计算黏土中Fe2O3、Al2O3的质量分数。
第6题
当以酚酞作指示剂时,用NaOH标准溶液测定某HCl溶液的浓度时,已知NaOH标液在保存时吸收了少量的CO2,对分析结果的影响将会______(偏高、偏低或无影响)。
第7题
A.以HCl标准溶液滴定某碱样,所用滴定管因未洗净,滴定时管内壁挂有液滴
B.以K2Cr2O7为基准物,用碘量法标定Na2S2O3溶液的浓度时,滴定速度过快,并过早读出滴定管读数
C.基准物在称量时吸湿了
D.以EDTA标准溶液滴定钙镁含量时,滴定速度过快
E.以失去部分结晶水的硼砂为基准物,标定盐酸溶液的浓度
第8题
第9题
第10题
A.以硫酸钡重量法测定钡时,沉淀剂硫酸加入量不足
B.以失去结晶水的硼砂为基准物质标定盐酸溶液的浓度
C.测定某石料中钙镁含量时,试样在称量时吸潮了
D.以重铬酸钾滴定亚铁时,酸式滴定管没有用重铬酸钾标准溶液荡洗
E.标定氢氧化钠溶液的邻苯二甲酸氢钾中含有少量邻苯二甲酸
第11题
抗坏血酸(维生素C,摩尔质量为176.1g·mol-1)能被I2定量氧化,其反应为
C6H8O6+I2====C6H6O6+2HI
取100.0mL柠檬汁样品用H2SO4酸化,并加入20.00mL 0.02500mol·L-1I2溶液,待反应完全后,过量的I2用0.01000mol·L-1Na2S2O3标准溶液10.00mL滴定至终点,计算每毫升柠檬水果汁中抗坏血酸的质量。