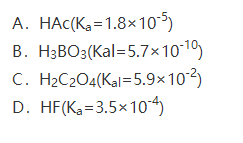题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
写出下列物质0.1mol/L水溶液的颜色:
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“写出下列物质0.1mol/L水溶液的颜色:”相关的问题
更多“写出下列物质0.1mol/L水溶液的颜色:”相关的问题
第1题
将下列水溶液按渗透压由大到小的顺序排列: (1)0.1mol/L KCl (2)0.1mol/L蔗糖 (3)0.2mol/L NaCl (4)0.3mol/L葡萄糖 (5)0.3mol/L KCl (6)0.3mol/L CaClz
第4题
问题1、自然界一切物质都具有能量,而且能量可以相互转化。从能量来看,电解是()转变为()的过程。能量的转化很多是以热量的形式出现的,例如甲烷作为一种清洁能源,标准状况下燃烧0.448L甲烷生成液态水,放出QKJ热量,写出该反应的热化学方程式()。问题2、写出电解饱和食盐水的离子方程式()。问题3、试预测离子交换膜法电解食盐水中离子交换膜可能的作用是()、()。问题4、电解熔融的氧化钠可以得到金属钠。写出该反应的化学方程式()。铝也可以用电解法得到,请用一个实验事实说明钠与铝的金属性强弱()。 问题5、室温下,0.1mol/LNaCIO溶液的pH()0.1mol/LNa2SO3溶液的pH。(选填“大于”、“小于”或“等于”)。浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为()。(酸性:H2SO3>H2CO3>HSO3->HCIO>HCO3-)。
第8题
A.0.1mol/L
B.0.2mol/L
C.0.4mol/L
D.0.6mol/L
第9题
A.甲醇为溶剂
B.结晶紫为指示剂
C.冰醋酸-醋酐为溶剂
D.高氯酸与硫酸奎宁的反应摩尔比为1∶1
E.高氯酸滴定液(0.1mol/L)
第10题
当下列各酸水溶液中的H+浓度(单位:mol/L)相等时,哪一种溶液中物质的量浓度最大?( )